Sālsskābes īpatnējā iztvaikošanas siltuma vērtība. Vāra. Īpatnējais iztvaikošanas siltums
Tiek saukts process, kurā viela tiek mainīta no šķidra stāvokļa uz gāzveida stāvokli iztvaikošana. Iztvaicēšanu var veikt divu procesu veidā: i.
Vāra
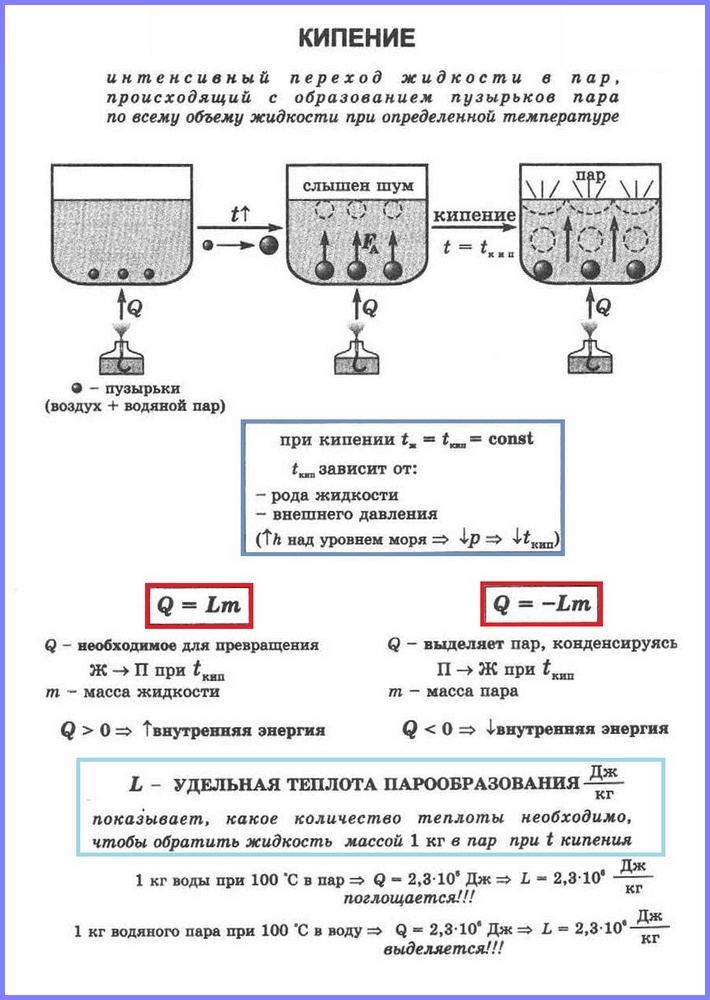
Otrais iztvaikošanas process ir vārīšanās. Jūs varat skatīties šo procesu ar vienkārša pieredzeūdens sildīšana stikla kolbā. Sildot ūdeni, tajā pēc brīža parādās burbuļi, kas satur gaisu un piesātinātus ūdens tvaikus, kas veidojas burbuļu iekšienē esošajam ūdenim iztvaikojot. Kad temperatūra paaugstinās, spiediens burbuļu iekšpusē palielinās, un peldspējas spēka ietekmē tie paceļas uz augšu. Taču, tā kā augšējos ūdens slāņos temperatūra ir zemāka nekā apakšējos, tvaiki burbuļos sāk kondensēties un tie saraujas. Kad ūdens sasilst visā tilpumā, burbuļi ar tvaiku paceļas virspusē, pārsprāgst un izplūst tvaiks. Ūdens vārās. Tas notiek temperatūrā, kurā spiediens piesātināts tvaiks burbuļi ir vienādi ar atmosfēras spiedienu.
Tiek saukts iztvaikošanas process, kas notiek visā šķidruma tilpumā noteiktā temperatūrā. Temperatūru, kurā šķidrums vārās, sauc vārīšanās punkts.
Šī temperatūra ir atkarīga no atmosfēras spiediena. Palielinoties atmosfēras spiedienam, paaugstinās viršanas temperatūra.
Pieredze rāda, ka viršanas procesā šķidruma temperatūra nemainās, neskatoties uz to, ka enerģija nāk no ārpuses. Šķidruma pāreja uz gāzveida stāvokli viršanas temperatūrā ir saistīta ar attāluma palielināšanos starp molekulām un attiecīgi ar pievilcības pārvarēšanu starp tām. Šķidrumam piegādātā enerģija tiek iztērēta, lai veiktu pievilkšanas spēku pārvarēšanas darbu. Tas notiek, līdz viss šķidrums pārvēršas tvaikos. Tā kā šķidrumam un tvaikiem viršanas laikā ir vienāda temperatūra, vidējā kinētiskā enerģija molekulas nemainās, tikai palielinās to potenciālā enerģija.
Attēlā parādīts ūdens temperatūras grafiks atkarībā no laika, kad tas tiek uzkarsēts no istabas temperatūras līdz vārīšanās temperatūrai (AB), vārīšanās (BC), sildīšana ar tvaiku (CD), tvaika dzesēšana (DE), kondensācija (EF) un sekojošā dzesēšana (FG).
Īpatnējais iztvaikošanas siltums
Dažādu vielu pārvēršanai no šķidra stāvokļa gāzveida stāvoklī ir nepieciešama dažāda enerģija, šo enerģiju raksturo vērtība, ko sauc par īpatnējo iztvaikošanas siltumu.
Īpašs karstums iztvaikošana (L) ir vērtība, kas vienāda ar siltuma daudzuma attiecību, kas jāpiešķir vielai, kuras masa ir 1 kg, lai tā viršanas temperatūrā no šķidra stāvokļa pārvērstos gāzveida stāvoklī.
Īpatnējā iztvaikošanas siltuma mērvienība ir [ L] = J/kg.
Lai aprēķinātu siltuma daudzumu Q, kas jāpiešķir vielai ar masu mn, lai tā no šķidra stāvokļa pārvērstos gāzveida stāvoklī, ir nepieciešams īpatnējais iztvaikošanas siltums ( L) reizināts ar vielas masu: Q = Lm.
Kad tvaiks kondensējas, izdalās noteikts siltuma daudzums, un tā vērtība ir vienāda ar siltuma daudzuma vērtību, kas jāiztērē, lai šķidrums tādā pašā temperatūrā pārvērstos tvaikā.
Lai uzturētu ūdens (vai cita šķidruma) vārīšanos, tam ir nepieciešams nepārtraukti pievadīt siltumu, piemēram, sildīt ar degli. Šajā gadījumā ūdens un trauka temperatūra nepaaugstinās, bet katrai laika vienībai veidojas noteikts daudzums tvaika. No tā izriet secinājums, ka ūdens pārvēršanai tvaikos ir nepieciešama siltuma pieplūde, tāpat kā tas notiek kristāla (ledus) pārtapšanas laikā šķidrumā (§ 269). Siltuma daudzumu, kas nepieciešams, lai šķidruma masas vienību pārvērstu tvaikos ar tādu pašu temperatūru, sauc par konkrētā šķidruma iztvaikošanas īpatnējo siltumu. To izsaka džoulos uz kilogramu.
Ir viegli saprast, ka, tvaikiem kondensējoties šķidrumā, ir jāizdalās tikpat daudz siltuma. Patiešām, nolaidīsim katlam pievienotu cauruli ūdens glāzē (488. att.). Kādu laiku pēc karsēšanas no ūdenī iegremdētās caurules gala sāks nākt ārā gaisa burbuļi. Šis gaiss nedaudz paaugstina ūdens temperatūru. Tad ūdens katlā uzvārās, pēc kā mēs redzēsim, ka burbuļi, kas izplūst no caurules gala, vairs neceļas augšā, bet ātri samazinās un asa skaņa pazust. Tie ir tvaika burbuļi, kas kondensējas ūdenī. Tiklīdz no katla gaisa vietā izplūst tvaiks, ūdens sāks ātri uzkarst. Kā īpašs karstums tvaiks ir aptuveni tāds pats kā gaiss, tad no šī novērojuma izriet, ka tik strauja ūdens uzkarsēšana notiek tieši tvaika kondensācijas dēļ.

Rīsi. 488. Kamēr no katla izplūst gaiss, termometrs rāda gandrīz tādu pašu temperatūru. Kad gaisa vietā izplūst tvaiks un tas sāk kondensēties krūzē, termometra stabiņš ātri paaugstināsies, norādot uz temperatūras paaugstināšanos.
Kad tvaika masas vienība kondensējas šķidrumā ar tādu pašu temperatūru, izdalās siltuma daudzums, kas vienāds ar īpatnējo iztvaikošanas siltumu. To varētu paredzēt, pamatojoties uz enerģijas nezūdamības likumu. Patiešām, ja tas tā nebūtu, tad būtu iespējams uzbūvēt mašīnu, kurā šķidrums vispirms iztvaiko un pēc tam kondensējas: starpība starp iztvaikošanas siltumu un kondensācijas siltumu atspoguļotu visu ķermeņu kopējās enerģijas pieaugumu. piedalās izskatāmajā procesā. Un tas ir pretrunā ar enerģijas nezūdamības likumu.
Īpatnējo iztvaikošanas siltumu var noteikt, izmantojot kalorimetru, līdzīgi kā tas tiek darīts, nosakot īpatnējo saplūšanas siltumu (§ 269). Ielejiet kalorimetrā noteiktu daudzumu ūdens un izmēra tā temperatūru. Pēc tam kādu laiku ūdenī ievadīsim testa šķidruma tvaikus no katla, veicot pasākumus, lai nodrošinātu, ka plūst tikai tvaiks, bez šķidruma pilieniem. Lai to izdarītu, tvaiks tiek izvadīts caur tvaikoni (489. att.). Pēc tam atkal mēra ūdens temperatūru kalorimetrā. Nosverot kalorimetru, pēc tā masas pieauguma varam spriest par tvaiku daudzumu, kas kondensējas šķidrumā.

Rīsi. 489. Sukhoparnik - ierīce ūdens pilienu aizturēšanai, kas pārvietojas kopā ar tvaiku
Izmantojot enerģijas nezūdamības likumu, mēs varam sastādīt šī procesa vienādojumu siltuma bilance, kas ļauj noteikt ūdens īpatnējo iztvaikošanas siltumu. Lai ūdens masa kalorimetrā (ieskaitot kalorimetra ūdens ekvivalentu) ir vienāda ar tvaika masu - , ūdens siltumietilpību - , ūdens sākotnējo un beigu temperatūru kalorimetrā - un , viršanas temperatūru ūdens - un īpatnējais iztvaikošanas siltums - . Siltuma bilances vienādojumam ir forma
![]() .
.
Dažu šķidrumu īpatnējā iztvaikošanas siltuma noteikšanas rezultāti normālā spiedienā ir doti tabulā. 20. Kā redzat, šis karstums ir diezgan liels. Lielajam ūdens iztvaikošanas siltumam dabā ir ārkārtīgi liela nozīme, jo dabā iztvaikošanas procesi notiek grandiozā mērogā.
20. tabula. Dažu šķidrumu īpatnējais iztvaikošanas siltums
|
Viela |
Viela |
||
|
etanols) |
|||
Ņemiet vērā, ka tabulā norādītās īpatnējā iztvaikošanas siltuma vērtības attiecas uz viršanas temperatūru plkst normāls spiediens. Ja šķidrums vārās vai vienkārši iztvaiko citā temperatūrā, tad tā īpatnējais iztvaikošanas siltums ir atšķirīgs. Paaugstinoties šķidruma temperatūrai, iztvaikošanas siltums vienmēr samazinās. Skaidrojumu tam apskatīsim vēlāk.
295.1. Aprēķiniet siltuma daudzumu, kas nepieciešams, lai uzsildītu 20 g ūdens līdz vārīšanās temperatūrai, un 20 g ūdens pārvērstu tvaikos pie .
295.2. Kādu temperatūru iegūs, ja glāzē, kurā ir 200 g ūdens, ievadīs 3 g tvaika pie ? Ignorējiet stikla siltumietilpību.
Mēs visi zinām, ka ūdens tējkannā vārās 100°C. Bet vai esat ievērojuši, ka vārīšanās procesā ūdens temperatūra nemainās? Jautājums ir – kur paliek saražotā enerģija, ja pastāvīgi turam tvertni ugunī? Tas pārvērš šķidrumu tvaikā. Tādējādi, lai ūdens pārietu gāzveida stāvoklī, ir nepieciešama pastāvīga siltuma padeve. Cik nepieciešams, lai kilograms šķidruma pārvērstu tādas pašas temperatūras tvaikā, nosaka fizikāls lielums, ko sauc par ūdens īpatnējo iztvaikošanas siltumu.
Daudzuma fiziskā nozīme
Vārīšanai ir nepieciešama enerģija. Lielāko daļu no tā izmanto, lai salauztu ķīmiskās saites starp atomiem un molekulām, kā rezultātā veidojas tvaika burbuļi, un mazākais iet tvaikus paplašināt, tas ir, lai izveidotie burbuļi varētu pārsprāgt un atbrīvot to. Tā kā šķidrums ieliek visu savu enerģiju pārejā uz gāzveida stāvokli, tā "spēki" izsīkst. Pastāvīgai enerģijas atjaunošanai un vārīšanās paildzināšanai traukā ar šķidrumu jāienes arvien vairāk siltuma. Tā pieplūdi var nodrošināt apkures katls, gāzes deglis vai kāds cits. sildīšanas ierīce. Vārīšanās laikā šķidruma temperatūra nepaaugstinās, notiek tādas pašas temperatūras tvaika veidošanās process.
Nepieciešami dažādi šķidrumi dažāda summa uzkarsē, lai pārvērstu tvaikā. Kurš - parāda īpatnējo iztvaikošanas siltumu.
Varat saprast, kā šī vērtība tiek noteikta, izmantojot piemēru. Ņem 1 litru ūdens un uzvāra. Pēc tam izmērām siltuma daudzumu, kas nepieciešams visa šķidruma iztvaicēšanai, un iegūstam ūdens īpatnējā iztvaikošanas siltuma vērtību. Par citiem ķīmiskie savienojumišis rādītājs būs atšķirīgs.
Fizikā apzīmē īpatnējo iztvaikošanas siltumu Latīņu burts L. To mēra džoulos uz kilogramu (J/kg). To var iegūt, iztvaikošanas laikā patērēto siltumu dalot ar šķidruma masu:
Šī vērtība ir ļoti svarīga ražošanas procesiem pamatā modernās tehnoloģijas. Piemēram, viņi no tā vadās metālu ražošanā. Izrādījās, ka, ja dzelzi izkausē un pēc tam kondensē, ar tālāku sacietēšanu veidojas stiprāks kristāla režģis.
Kas ir vienāds ar
laikā tika noteikta īpatnējā siltuma vērtība dažādām vielām (r). laboratorijas pētījumi. Ūdens normālā stāvoklī atmosfēras spiediens vārās 100 °C, un ūdens iztvaikošanas siltums ir 2258,2 kJ/kg. Šis rādītājs dažām citām vielām ir norādīts tabulā:
| Viela | viršanas temperatūra, °C | r, kJ/kg |
|---|---|---|
| Slāpeklis | -196 | 198 |
| Hēlijs | -268,94 | 20,6 |
| Ūdeņradis | -253 | 454 |
| Skābeklis | -183 | 213 |
| Ogleklis | 4350 | 50000 |
| Fosfors | 280 | 400 |
| Metāns | -162 | 510 |
| Pentāns | 36 | 360 |
| Dzelzs | 2735 | 6340 |
| Varš | 2590 | 4790 |
| Alva | 2430 | 2450 |
| Svins | 1750 | 8600 |
| Cinks | 907 | 1755 |
| Merkurs | 357 | 285 |
| Zelts | 2 700 | 1 650 |
| Etanols | 78 | 840 |
| Metilspirts | 65 | 1100 |
| Hloroforms | 61 | 279 |
Tomēr šis rādītājs var mainīties noteiktu faktoru ietekmē:
- Temperatūra. Palielinoties, iztvaikošanas siltums samazinās un var būt nulle.
t, °C r, kJ/kg 2500 10 2477 20 2453 50 2380 80 2308 100 2258 200 1940 300 1405 374 115 374,15 - Spiediens. Samazinoties spiedienam, palielinās iztvaikošanas siltums un otrādi. Viršanas punkts ir tieši proporcionāls spiedienam un var sasniegt kritisko vērtību 374 °C.
p, Pa bp, °C r, kJ/kg 0,0123 10 2477 0,1234 50 2380 1 100 2258 2 120 2202 5 152 2014 10 180 1889 20 112 1638 50 264 1638 100 311 1316 200 366 585 220 373,7 184,8 Kritiskais 221,29 374,15 - - Vielas masa. Procesā iesaistītā siltuma daudzums ir tieši proporcionāls iegūtā tvaika masai.
Iztvaikošanas un kondensācijas attiecība
Fiziķi atklājuši, ka apgrieztās iztvaikošanas procesā – kondensācijā – tvaiks tērē tieši tādu pašu enerģijas daudzumu, kāds tika iztērēts tā veidošanai. Šis novērojums apstiprina enerģijas nezūdamības likumu.
Pretējā gadījumā būtu iespējams izveidot instalāciju, kurā šķidrums iztvaikotu un pēc tam kondensētos. Atšķirība starp iztvaikošanai nepieciešamo siltumu un kondensācijai pietiekamo siltumu izraisītu enerģijas uzkrāšanos, ko varētu izmantot citiem mērķiem. Patiesībā tiktu izveidota mūžīgā kustība. Bet tas ir pretrunā ar fiziskajiem likumiem un tāpēc neiespējami.
Kā tas tiek mērīts
- Ūdens īpatnējo iztvaikošanas siltumu eksperimentāli mēra fizikālās laboratorijās. Šim nolūkam tiek izmantoti kalorimetri. Procedūra ir šāda:
- Kalorimetrā ielej noteiktu daudzumu šķidruma.
Vārīšanās ir intensīva iztvaikošana, kas notiek, kad šķidrums tiek uzkarsēts ne tikai no virsmas, bet arī no tā iekšpuses.
Vārīšanās notiek, absorbējot siltumu.
Lielākā daļa no piegādātā siltuma tiek tērēts saišu pārraušanai starp vielas daļiņām, pārējais tiek tērēts darbam, kas veikts tvaika izplešanās laikā.
Tā rezultātā mijiedarbības enerģija starp tvaiku daļiņām kļūst lielāka nekā starp šķidruma daļiņām, tāpēc tvaika iekšējā enerģija ir lielāka par šķidruma iekšējo enerģiju tajā pašā temperatūrā.
Siltuma daudzumu, kas nepieciešams šķidruma pārnešanai uz tvaikiem viršanas procesā, var aprēķināt, izmantojot formulu:

kur m ir šķidruma masa (kg),
L ir īpatnējais iztvaikošanas siltums.
Īpatnējais iztvaikošanas siltums parāda, cik daudz siltuma nepieciešams, lai 1 kg dotās vielas pārvērstu tvaikā viršanas temperatūrā. Īpatnējā iztvaikošanas siltuma mērvienība SI sistēmā:
[ L ] = 1 J/kg
Palielinoties spiedienam, paaugstinās šķidruma viršanas temperatūra, samazinās īpatnējais iztvaikošanas siltums un otrādi.

Vārīšanās laikā šķidruma temperatūra nemainās.
Viršanas temperatūra ir atkarīga no spiediena, kas tiek iedarbināts uz šķidrumu.
Katrai vielai pie tāda paša spiediena ir savs viršanas punkts.
Palielinoties atmosfēras spiedienam, vārīšanās sākas vairāk paaugstināta temperatūra, otrādi, kad spiediens samazinās.
Piemēram, ūdens vārās 100°C tikai normālā atmosfēras spiedienā.
KAS NOTIEK ŠĶIDRUMĀ VAIROŠANĀ?

Vārīšanās ir šķidruma pāreja tvaikos ar nepārtrauktu tvaika burbuļu veidošanos un augšanu šķidrumā, kurā šķidrums iztvaiko. Sildīšanas sākumā ūdens ir piesātināts ar gaisu un tam ir istabas temperatūra. Sildot ūdeni, tajā izšķīdinātā gāze izdalās trauka dibenā un sieniņās, veidojot gaisa burbuļus. Tie sāk parādīties ilgi pirms vārīšanās. Ūdens iztvaiko šajos burbuļos. Burbulis, kas piepildīts ar tvaiku, sāk uzpūsties pietiekami augstā temperatūrā.

Sasniedzot noteikti izmēri tas atraujas no dibena, paceļas līdz ūdens virsmai un pārsprāgst. Šajā gadījumā tvaiki atstāj šķidrumu. Ja ūdens nav pietiekami uzsildīts, tvaika burbulis, paceļoties aukstajos slāņos, sabrūk. Iegūtās ūdens svārstības noved pie tā, ka visā ūdens tilpumā parādās milzīgs skaits mazu gaisa burbuļu: tā sauktā "baltā atslēga".

Iedarbojas gaisa burbulis ar tilpumu trauka apakšā celšanas spēks:
Fpod \u003d Farhimēds — gravitācija
Burbulis tiek nospiests līdz apakšai, jo spiediena spēki nedarbojas uz apakšējo virsmu. Sildot, burbulis izplešas, jo tajā izplūst gāze, un atraujas no apakšas, kad pacelšanas spēks ir nedaudz lielāks par nospiešanas spēku. Burbuļa izmērs, kas var atrauties no apakšas, ir atkarīgs no tā formas. Burbuļu formu apakšā nosaka trauka dibena mitrināmība.
Neviendabīguma mitrināšana un burbuļu saplūšana apakšā izraisīja to lieluma palielināšanos. Plkst lieli izmēri Kad aiz tā paceļas burbulis, veidojas tukšumi, spraugas un virpuļi.
Kad burbulis pārsprāgst, viss apkārt esošais šķidrums plūst uz iekšu, un rodas gredzenveida vilnis. Aizverot, viņa izmet ūdens stabu.

Kad plīstošie burbuļi sabrūk šķidrumā, izplatās ultraskaņas frekvenču triecienviļņi, ko pavada dzirdams troksnis. Priekš sākuma posmi vārīšanai raksturīgas visskaļākās un augstākās skaņas ("baltās atslēgas" stadijā tējkanna "dzied").
(avots: virlib.eunnet.net)
ŪDENS AGREGĀTU STĀVOKĻU IZMAIŅU TEMPERATŪRAS GRĀFIKS

SKATĪTIES GRĀMATŪTĀ!
INTERESANTI
Kāpēc tējkannas vākā ir caurums?
Lai atbrīvotu tvaiku. Ja vākā nav cauruma, tvaiks var izšļakstīt ūdeni pāri tējkannas snīpim.
___
Kartupeļu gatavošanas ilgums, sākot no vārīšanās brīža, nav atkarīgs no sildītāja jaudas. Ilgumu nosaka produkta uzturēšanās laiks viršanas temperatūrā.
Sildītāja jauda neietekmē viršanas temperatūru, bet tikai ūdens iztvaikošanas ātrumu.
Vārīšana var izraisīt ūdens sasalšanu. Lai to izdarītu, no trauka, kurā atrodas ūdens, ir nepieciešams izsūknēt gaisu un ūdens tvaikus, lai ūdens visu laiku vārītos.
"Kadi viegli vārās pāri malai - uz sliktiem laikapstākļiem!"
Atmosfēras spiediena kritums, kas pavada laikapstākļu pasliktināšanos, ir iemesls, kāpēc piens "aiztek" ātrāk.
___
Ļoti karstu verdošu ūdeni var iegūt dziļo raktuvju apakšā, kur gaisa spiediens ir daudz lielāks nekā uz Zemes virsmas. Tātad 300 m dziļumā ūdens vārīsies 101 ͦ C temperatūrā. Ar gaisa spiedienu 14 atmosfēras ūdens vārās 200 ͦ C temperatūrā.
Zem gaisa sūkņa zvana var iegūt "verdošu ūdeni" 20 ͦ C temperatūrā.
Uz Marsa mēs dzeram "verdošu ūdeni" 45 C temperatūrā.
Sālsūdens vārās virs 100 ͦ C. ___
Kalnu reģionos ievērojamā augstumā zem pazemināta atmosfēras spiediena ūdens vārās temperatūrā, kas ir zemāka par 100 ͦ Celsija.

Gaidīšana, līdz šāda maltīte tiks pagatavota, aizņem ilgāku laiku.
Lej aukstu ... un tas uzvārīsies!
Parasti ūdens vārās 100 grādos pēc Celsija. Uzkarsē ūdeni kolbā uz degļa līdz vārīšanās temperatūrai. Izslēgsim degli. Ūdens pārstāj vārīties. Mēs aizveram kolbu ar aizbāzni un sākam uzmanīgi ielej aukstu ūdeni uz aizbāžņa. Kas tas ir? Ūdens atkal vārās!
..............................zem strūklas auksts ūdens nedaudz ūdens kolbā, un līdz ar to ūdens tvaiki sāk atdzist.
Tvaika tilpums samazinās un spiediens virs ūdens virsmas mainās...
Kā jūs domājat, kurā virzienā?
... Ūdens viršanas temperatūra pazeminātā spiedienā ir mazāka par 100 grādiem, un ūdens kolbā atkal vārās!
____
Gatavojot, spiediens katlā - "spiedienkatlā" - ir aptuveni 200 kPa, un zupa šādā katlā izcepsies daudz ātrāk.
Jūs varat ievilkt ūdeni šļircē līdz apmēram pusei, aizvērt to ar to pašu korķi un strauji pavelciet virzuli. Ūdenī parādīsies daudz burbuļu, kas norāda, ka ir sācies ūdens vārīšanās process (un tas ir istabas temperatūrā!).
___
Kad viela nonāk gāzveida stāvoklī, tās blīvums samazinās apmēram 1000 reizes.
___
Pirmajām elektriskajām tējkannām zem apakšas bija sildītāji. Ūdens nesaskārās ar sildītāju un vārījās ļoti ilgi. 1923. gadā Arturs Large veica atklājumu: viņš ievietoja sildītāju īpašā vara caurulē un ievietoja to tējkannā. Ūdens ātri uzvārījās.
ASV ir izstrādātas pašatdzesējošas kannas bezalkoholiskajiem dzērieniem. Burkā ir uzstādīts nodalījums ar zemu vārīšanās temperatūru. Sasmalcinot kapsulu karstā dienā, šķidrums sāks strauji vārīties, atņemot siltumu no burciņas satura, un 90 sekunžu laikā dzēriena temperatūra pazeminās par 20-25 grādiem pēc Celsija.
KĀPĒC?
Vai, jūsuprāt, ir iespējams cieti novārīt olu, ja ūdens vārās temperatūrā, kas zemāka par 100 grādiem pēc Celsija?
____
Vai ūdens vārīsies katlā, kas peld citā katlā ar verdošu ūdeni?
Kāpēc? ___
Vai var likt ūdenim vārīties, to nesildot?

Vārīšanās, kā redzējām, arī ir iztvaikošana, tikai to pavada strauja tvaika burbuļu veidošanās un augšana. Ir skaidrs, ka vārīšanās laikā šķidrumam ir nepieciešams ievest noteiktu siltuma daudzumu. Šis siltuma daudzums tiek novirzīts tvaika veidošanai. Turklāt dažādiem vienas masas šķidrumiem ir nepieciešams atšķirīgs siltuma daudzums, lai tie viršanas temperatūrā pārvērstos tvaikos.
Eksperimenti ir parādījuši, ka 1 kg smaga ūdens iztvaikošana 100 °C temperatūrā prasa 2,3 x 10 6 J enerģijas. Lai iztvaicētu 1 kg ētera 35 °C temperatūrā, nepieciešams 0,4 10 6 J enerģijas.
Tāpēc, lai iztvaikojošā šķidruma temperatūra nemainītos, šķidrumam jāpavada noteikts siltuma daudzums.
Fizikālo lielumu, kas parāda, cik daudz siltuma nepieciešams, lai šķidrums ar masu 1 kg, nemainot temperatūru, pārvērstos tvaikos, tiek saukts par īpatnējo iztvaikošanas siltumu.
Īpatnējo iztvaikošanas siltumu apzīmē ar burtu L. Tā mērvienība ir 1 J/kg.
Eksperimentos noskaidrots, ka ūdens īpatnējais iztvaikošanas siltums 100 °C temperatūrā ir 2,3 10 6 J/kg. Citiem vārdiem sakot, ir nepieciešams 2,3 x 10 6 J enerģijas, lai 1 kg ūdens pārvērstu tvaikā 100 °C temperatūrā. Tāpēc viršanas temperatūrā vielas iekšējā enerģija tvaika stāvoklī ir lielāka par tādas pašas masas vielas iekšējo enerģiju šķidrā stāvoklī.
6. tabula
Dažu vielu īpatnējais iztvaikošanas siltums (viršanas temperatūrā un normālā atmosfēras spiedienā)
Saskaroties ar aukstu priekšmetu, ūdens tvaiki kondensējas (25. att.). Šajā gadījumā tiek atbrīvota tvaika veidošanās laikā absorbētā enerģija. Precīzi eksperimenti liecina, ka, kondensējoties, tvaiks izdala tādu enerģijas daudzumu, kāds nonāca tā veidošanā.

Rīsi. 25. Tvaika kondensācija
Līdz ar to, 1 kg ūdens tvaiku 100 °C temperatūrā pārvēršot par tādas pašas temperatūras ūdeni, atbrīvojas 2,3 x 10 6 J enerģijas. Kā redzams no salīdzinājuma ar citām vielām (6. tabula), šī enerģija ir diezgan augsta.
Var izmantot enerģiju, kas izdalās tvaika kondensācijas laikā. Lielajās termoelektrostacijās turbīnās izmantotais tvaiks silda ūdeni.
Šādi uzsildīts ūdens tiek izmantots ēku apkurei, vannās, veļas mazgātavās un citām sadzīves vajadzībām.
Lai aprēķinātu siltuma daudzumu Q, kas nepieciešams, lai jebkuras masas šķidrumu, kas ņemts viršanas temperatūrā, pārvērstu tvaikos, īpatnējais iztvaikošanas siltums L jāreizina ar masu m:
Pēc šīs formulas var noteikt, ka
m = Q/L, L = Q/m
Siltuma daudzumu, ko izdala tvaiki ar masu m, kondensējoties viršanas temperatūrā, nosaka pēc tās pašas formulas.
Piemērs. Cik daudz enerģijas ir nepieciešams, lai 2 kg ūdens 20°C pārvērstu tvaikos? Pierakstīsim problēmas stāvokli un atrisināsim to.

Jautājumi
- Kāda enerģija tiek piegādāta šķidrumam vārīšanās laikā?
- Kāds ir īpatnējais iztvaikošanas siltums?
- Kā var eksperimentāli parādīt, ka tvaika kondensācijas laikā izdalās enerģija?
- Kādu enerģiju kondensācijas laikā izdala 1 kg ūdens tvaiku?
- Kur tehnoloģijā tiek izmantota ūdens tvaiku kondensācijas laikā atbrīvotā enerģija?
16. vingrinājums
- Kā saprast, ka ūdens īpatnējais iztvaikošanas siltums ir 2,3 10 6 J/kg?
- Kā saprast, ka amonjaka īpatnējais kondensācijas siltums ir 1,4 10 6 J/kg?
- Kurām no 6. tabulā minētajām vielām, pārvēršot no šķidra stāvokļa tvaikos, iekšējā enerģija palielinās vairāk? Pamato atbildi.
- Cik daudz enerģijas ir nepieciešams, lai 150 g ūdens pārvērstu tvaikos 100°C temperatūrā?
- Cik daudz enerģijas jāpatērē, lai uzvārītu un iztvaicētu ūdeni ar masu 5 kg, kas ņemts 0 °C temperatūrā?
- Kādu enerģijas daudzumu izdalīs ūdens, kura masa ir 2 kg, atdzesējot no 100 līdz 0 °C? Kāds enerģijas daudzums izdalīsies, ja ūdens vietā ņemsim tikpat daudz tvaika 100 °C temperatūrā?
Exercise
- Saskaņā ar 6. tabulu nosakiet, kuras no vielām, pārvēršoties no šķidra stāvokļa tvaikos, iekšējā enerģija palielinās spēcīgāk. Pamato atbildi.
- Sagatavojiet ziņojumu par kādu no tēmām (pēc izvēles).
- Kā veidojas rasa, sals, lietus un sniegs.
- Ūdens cikls dabā.
- Metāla liešana.
