Wartość ciepła właściwego parowania kwasu solnego. Wrzenie. Ciepło właściwe waporyzacji
Nazywa się proces zmiany substancji ze stanu ciekłego w stan gazowy odparowanie. Waporyzację można przeprowadzić w dwóch procesach:
Wrzenie
Drugim procesem waporyzacji jest gotowanie. Możesz oglądać ten proces za pomocą proste doświadczenie podgrzewanie wody w szklanej kolbie. Po podgrzaniu wody po pewnym czasie pojawiają się w niej bąbelki, które zawierają powietrze i nasyconą parę wodną, która powstaje podczas parowania wody wewnątrz bąbelków. Wraz ze wzrostem temperatury wzrasta ciśnienie wewnątrz pęcherzyków, które pod wpływem siły wyporu rosną. Ponieważ jednak temperatura górnych warstw wody jest niższa niż dolnych, para w bąbelkach zaczyna się skraplać i kurczyć. Gdy woda nagrzeje się w całej objętości, bąbelki z parą unoszą się na powierzchnię, pękają i wydobywa się para. Woda się gotuje. Dzieje się to w temperaturze, w której ciśnienie para nasycona pęcherzyki są równe ciśnieniu atmosferycznemu.
Nazywa się proces parowania zachodzący w całej objętości cieczy w określonej temperaturze. Nazywa się temperaturę wrzenia cieczy temperatura wrzenia.
Ta temperatura zależy od ciśnienia atmosferycznego. Wraz ze wzrostem ciśnienia atmosferycznego wzrasta temperatura wrzenia.
Doświadczenie pokazuje, że podczas procesu gotowania temperatura cieczy nie zmienia się, mimo że energia pochodzi z zewnątrz. Przejście cieczy w stan gazowy w temperaturze wrzenia wiąże się ze wzrostem odległości między cząsteczkami, a zatem z przezwyciężeniem przyciągania między nimi. Energia dostarczana do płynu jest zużywana na wykonanie pracy polegającej na przezwyciężeniu sił przyciągania. Dzieje się tak, dopóki cała ciecz nie zamieni się w parę. Ponieważ ciecz i para podczas gotowania mają tę samą temperaturę, średnia energia kinetyczna cząsteczki się nie zmieniają, zwiększa się tylko ich energia potencjalna.
Rysunek przedstawia wykres temperatury wody w funkcji czasu podczas jej ogrzewania od temperatury pokojowej do wrzenia (AB), wrzenia (BC), ogrzewania parą (CD), chłodzenia parą (DE), kondensacji (EF) i późniejszego chłodzenia (FG).
Ciepło właściwe waporyzacji
Do przekształcenia różnych substancji ze stanu ciekłego w stan gazowy potrzebna jest inna energia, energia ta charakteryzuje się wartością zwaną ciepłem właściwym parowania.
Ciepło właściwe odparowanie (L) jest wartością równą stosunkowi ilości ciepła, które musi zostać przekazane substancji o masie 1 kg, aby przekształcić ją ze stanu ciekłego w stan gazowy w temperaturze wrzenia.
Jednostką ciepła właściwego parowania jest [ L] = J/kg.
Aby obliczyć ilość ciepła Q, którą należy przekazać substancji o masie mn w celu jej przekształcenia ze stanu ciekłego w gazowy, konieczne jest posiadanie ciepła właściwego parowania ( L) razy masa substancji: Q = Lm.
Kiedy para się skrapla, uwalniana jest pewna ilość ciepła, a jej wartość jest równa wartości ilości ciepła, które należy wydać, aby zamienić ciecz w parę o tej samej temperaturze.
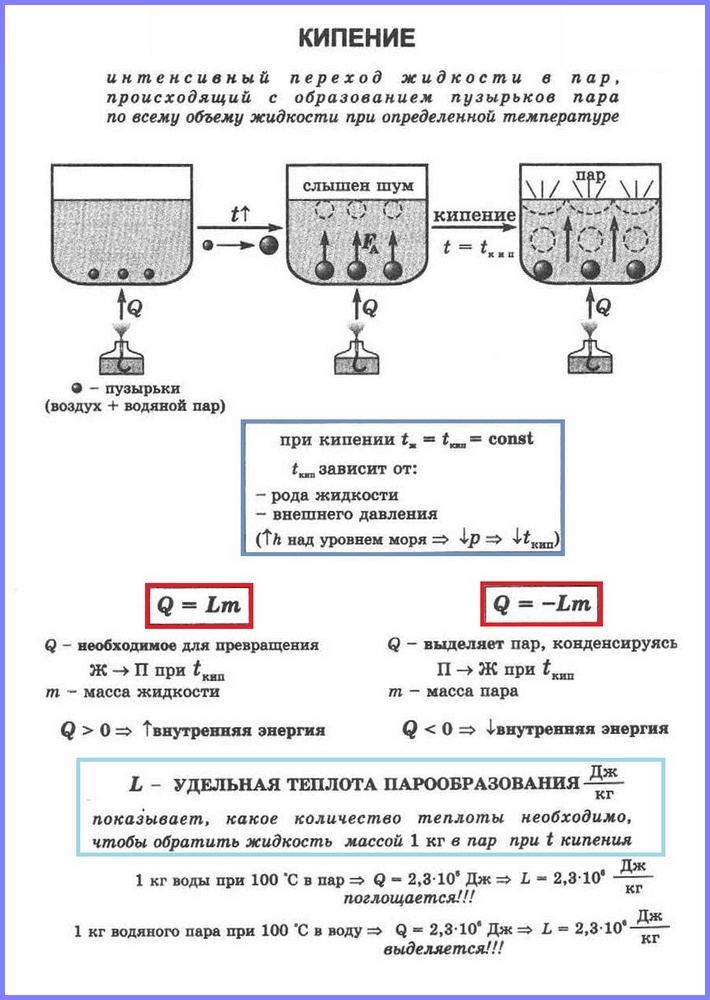
W celu utrzymania wrzenia wody (lub innej cieczy) konieczne jest ciągłe dostarczanie do niej ciepła, na przykład podgrzewanie palnikiem. W tym przypadku temperatura wody i naczynia nie wzrasta, ale na każdą jednostkę czasu powstaje pewna ilość pary. Z tego wynika wniosek, że przemiana wody w parę wymaga dopływu ciepła, tak jak ma to miejsce podczas przemiany kryształu (lód) w ciecz (§ 269). Ilość ciepła potrzebna do przekształcenia masy jednostkowej cieczy w parę o tej samej temperaturze nazywana jest ciepłem parowania danej cieczy. Wyrażana jest w dżulach na kilogram.
Łatwo zauważyć, że ta sama ilość ciepła musi zostać uwolniona, gdy para skrapla się w ciecz. Rzeczywiście, opuśćmy rurkę podłączoną do kotła do szklanki wody (ryc. 488). Jakiś czas po rozpoczęciu ogrzewania z końcówki zanurzonej w wodzie rurki zaczną wydobywać się bąbelki powietrza. Powietrze to nieznacznie podnosi temperaturę wody. Wtedy woda w bojlerze się zagotuje, po czym zobaczymy, że bąbelki wychodzące z końca rurki już nie unoszą się, ale szybko maleją i ostry dźwięk zniknąć. Są to bąbelki pary kondensującej się w wodzie. Gdy tylko z bojlera zamiast powietrza wydostanie się para, woda zacznie się szybko nagrzewać. Jak ciepło właściwe para jest w przybliżeniu taka sama jak powietrze, to z tej obserwacji wynika, że tak szybkie nagrzewanie wody następuje właśnie z powodu kondensacji pary.

Ryż. 488. Gdy powietrze wychodzi z kotła, termometr pokazuje prawie taką samą temperaturę. Kiedy para zamiast powietrza zacznie się skraplać w kubku, termometr szybko się podniesie, wskazując na wzrost temperatury.
Kiedy jednostka masy pary kondensuje się w ciecz o tej samej temperaturze, ilość ciepła jest uwalniana równą właściwemu ciepłu parowania. Można to przewidzieć na podstawie prawa zachowania energii. Rzeczywiście, gdyby tak nie było, można by zbudować maszynę, w której ciecz najpierw wyparowuje, a następnie skrapla się: różnica między ciepłem parowania a ciepłem kondensacji reprezentuje przyrost całkowitej energii wszystkich ciał udział w rozważanym procesie. A to jest sprzeczne z prawem zachowania energii.
Ciepło właściwe parowania można określić za pomocą kalorymetru, podobnie jak przy określaniu ciepła właściwego topnienia (§ 269). Wlej odpowiednią ilość wody do kalorymetru i zmierz jego temperaturę. Następnie przez jakiś czas będziemy wprowadzać do wody parę badanej cieczy z kotła, dokładając starań, aby przepływała tylko para, bez kropelek cieczy. W tym celu para przechodzi przez parowiec (ryc. 489). Następnie ponownie mierzymy temperaturę wody w kalorymetrze. Ważąc kalorymetr, możemy ocenić po wzroście jego masy ilość pary skondensowanej w ciecz.

Ryż. 489. Sukhoparnik - urządzenie do zatrzymywania kropel wody poruszających się wraz z parą
Korzystając z prawa zachowania energii, możemy skomponować równanie dla tego procesu bilans cieplny, który pozwala określić ciepło właściwe parowania wody. Niech masa wody w kalorymetrze (w tym odpowiednik wody w kalorymetrze) będzie równa masie pary - , pojemności cieplnej wody - , początkowej i końcowej temperaturze wody w kalorymetrze - oraz , temperaturze wrzenia woda - i ciepło właściwe parowania - . Równanie bilansu cieplnego ma postać
![]() .
.
Wyniki wyznaczania ciepła właściwego parowania niektórych cieczy pod ciśnieniem normalnym podano w tabeli. 20. Jak widać, ciepło to jest dość duże. Wysokie ciepło parowania wody odgrywa w przyrodzie niezwykle ważną rolę, ponieważ procesy parowania zachodzą w przyrodzie na ogromną skalę.
Tabela 20. Ciepło właściwe parowania niektórych cieczy
|
Substancja |
Substancja |
||
|
Etanol) |
|||
Należy pamiętać, że wartości ciepła właściwego parowania zawarte w tabeli odnoszą się do temperatury wrzenia w normalne ciśnienie. Jeżeli ciecz wrze lub po prostu odparuje w innej temperaturze, to jej ciepło właściwe parowania jest inne. Wraz ze wzrostem temperatury cieczy ciepło parowania zawsze maleje. Wyjaśnieniu tego przyjrzymy się później.
295.1. Oblicz ilość ciepła potrzebnego do podgrzania 20 g wody do temperatury wrzenia i zamienienia 20 g wody w parę w .
295.2. Jaką temperaturę uzyskamy, jeśli do szklanki zawierającej 200 g wody wprowadzi się 3 g pary o temperaturze ? Zignoruj pojemność cieplną szkła.
Wszyscy wiemy, że woda w czajniku wrze w 100°C. Ale czy zauważyłeś, że temperatura wody nie zmienia się podczas gotowania? Pytanie brzmi – dokąd trafia wytworzona energia, jeśli cały czas utrzymujemy w ogniu pojemnik? Przekształca ciecz w parę. Dlatego do przejścia wody w stan gazowy wymagany jest stały dopływ ciepła. Ile potrzeba, aby zamienić kilogram cieczy w parę o tej samej temperaturze, określa wielkość fizyczna zwana ciepłem właściwym parowania wody.
Fizyczne znaczenie ilości
Gotowanie wymaga energii. Większość z nich służy do łamania wiązania chemiczne między atomami i cząsteczkami, w wyniku czego powstają bąbelki pary, a ten mniejszy rozpręża parę, czyli tak, aby powstałe bąbelki mogły pęknąć i ją uwolnić. Ponieważ ciecz wkłada całą swoją energię w przejście w stan gazowy, jej „siły” się wyczerpują. Aby stale odnawiać energię i przedłużyć wrzenie, do pojemnika z płynem należy doprowadzać coraz więcej ciepła. Kocioł, palnik gazowy lub inny może zapewnić jego dopływ. Urządzenie ogrzewcze. Podczas gotowania temperatura cieczy nie wzrasta, zachodzi proces powstawania pary o tej samej temperaturze.
Różne płyny wymagają inna kwota ciepło do konwersji na parę. Który – pokazuje ciepło właściwe waporyzacji.
Możesz zrozumieć, jak ta wartość jest określana na przykładzie. Weź 1 litr wody i zagotuj. Następnie mierzymy ilość ciepła potrzebną do odparowania całej cieczy i otrzymujemy wartość ciepła właściwego parowania wody. Dla innych związki chemiczne ten wskaźnik będzie inny.
W fizyce oznacza się ciepło właściwe parowania łacińska litera L. Jest mierzony w dżulach na kilogram (J/kg). Można ją obliczyć dzieląc ciepło wydatkowane podczas parowania przez masę cieczy:
Ta wartość jest bardzo ważna dla procesy produkcji na podstawie nowoczesne technologie. Na przykład kierują się nią przy produkcji metali. Okazało się, że jeśli żelazo zostanie stopione, a następnie skondensowane, przy dalszym twardnieniu powstaje silniejsza sieć krystaliczna.
Co jest równe
Wartość ciepła właściwego dla różnych substancji (r) została wyznaczona podczas badania laboratoryjne. Woda w normie ciśnienie atmosferyczne wrze w 100°C, a ciepło parowania wody wynosi 2258,2 kJ/kg. Ten wskaźnik dla niektórych innych substancji podano w tabeli:
| Substancja | temperatura wrzenia, °C | r, kJ/kg |
|---|---|---|
| Azot | -196 | 198 |
| Hel | -268,94 | 20,6 |
| Wodór | -253 | 454 |
| Tlen | -183 | 213 |
| Węgiel | 4350 | 50000 |
| Fosfor | 280 | 400 |
| Metan | -162 | 510 |
| Pentan | 36 | 360 |
| Żelazo | 2735 | 6340 |
| Miedź | 2590 | 4790 |
| Cyna | 2430 | 2450 |
| Prowadzić | 1750 | 8600 |
| Cynk | 907 | 1755 |
| Rtęć | 357 | 285 |
| Złoto | 2 700 | 1 650 |
| Etanol | 78 | 840 |
| Alkohol metylowy | 65 | 1100 |
| Chloroform | 61 | 279 |
Jednak ten wskaźnik może się zmienić pod wpływem pewnych czynników:
- Temperatura. Wraz ze wzrostem ciepło parowania maleje i może być zero.
t, °C r, kJ/kg 2500 10 2477 20 2453 50 2380 80 2308 100 2258 200 1940 300 1405 374 115 374,15 - Nacisk. Wraz ze spadkiem ciśnienia wzrasta ciepło parowania i odwrotnie. Temperatura wrzenia jest wprost proporcjonalna do ciśnienia i może osiągnąć wartość krytyczną 374°C.
p, Pa temperatura wrzenia, °C r, kJ/kg 0,0123 10 2477 0,1234 50 2380 1 100 2258 2 120 2202 5 152 2014 10 180 1889 20 112 1638 50 264 1638 100 311 1316 200 366 585 220 373,7 184,8 Krytyczny 221,29 374,15 - - Masa substancji. Ilość ciepła zaangażowana w proces jest wprost proporcjonalna do masy powstałej pary.
Stosunek parowania i kondensacji
Fizycy odkryli, że proces odwrotnego parowania - kondensacji - para zużywa dokładnie taką samą ilość energii, jaka została zużyta na jej tworzenie. Ta obserwacja potwierdza prawo zachowania energii.
W przeciwnym razie możliwe byłoby stworzenie instalacji, w której ciecz wyparowałaby, a następnie uległaby skropleniu. Różnica między ciepłem wymaganym do parowania a ciepłem wystarczającym do kondensacji spowodowałaby akumulację energii, którą można by wykorzystać do innych celów. W rzeczywistości powstałaby maszyna perpetuum mobile. Ale jest to sprzeczne z prawami fizycznymi, a zatem niemożliwe.
Jak to się mierzy?
- Ciepło właściwe parowania wody jest mierzone eksperymentalnie w laboratoriach fizycznych. W tym celu stosuje się kalorymetry. Procedura wygląda następująco:
- Do kalorymetru wlewa się pewną ilość płynu.
Wrzenie to intensywne parowanie, które następuje, gdy ciecz jest podgrzewana nie tylko z powierzchni, ale także z jej wnętrza.
Wrzenie następuje wraz z pochłanianiem ciepła.
Większość dostarczonego ciepła zużywa się na zerwanie wiązań między cząsteczkami substancji, reszta jest zużywana na pracę wykonaną podczas rozprężania pary.
W rezultacie energia interakcji między cząstkami pary staje się większa niż między cząstkami cieczy, więc energia wewnętrzna pary jest większa niż energia wewnętrzna cieczy w tej samej temperaturze.
Ilość ciepła potrzebną do przekształcenia cieczy w parę podczas procesu wrzenia można obliczyć za pomocą wzoru:

gdzie m jest masą cieczy (kg),
L to ciepło właściwe parowania.
Ciepło właściwe waporyzacji pokazuje, ile ciepła potrzeba, aby zamienić 1 kg danej substancji w parę o temperaturze wrzenia. Jednostka ciepła właściwego parowania w układzie SI:
[ L ] = 1 J/kg
Wraz ze wzrostem ciśnienia wzrasta temperatura wrzenia cieczy, a ciepło właściwe parowania maleje i odwrotnie.

Podczas gotowania temperatura cieczy nie zmienia się.
Temperatura wrzenia zależy od ciśnienia wywieranego na ciecz.
Każda substancja pod tym samym ciśnieniem ma swoją własną temperaturę wrzenia.
Wraz ze wzrostem ciśnienia atmosferycznego wrzenie zaczyna się o więcej wysoka temperatura, na odwrót, gdy ciśnienie spada.
Na przykład woda wrze w temperaturze 100°C tylko przy normalnym ciśnieniu atmosferycznym.
CO DZIEJE SIĘ WE WNĘTRZU PŁYNU PODCZAS GOTOWANIA?

Wrzenie to przejście cieczy w parę z ciągłym tworzeniem i wzrostem pęcherzyków pary w cieczy, wewnątrz której ciecz odparowuje. Na początku ogrzewania woda jest nasycona powietrzem i ma temperaturę pokojową. Gdy woda jest podgrzewana, rozpuszczony w niej gaz uwalnia się na dnie i ściany naczynia, tworząc pęcherzyki powietrza. Zaczynają pojawiać się na długo przed gotowaniem. Woda paruje w te bąbelki. Pęcherzyk wypełniony parą zaczyna się nadmuchiwać w wystarczająco wysokiej temperaturze.

Osiągnięcie niektóre rozmiary odrywa się od dna, unosi się na powierzchnię wody i pęka. W takim przypadku para opuszcza ciecz. Jeśli woda nie zostanie wystarczająco podgrzana, pęcherzyk pary, unoszący się w zimne warstwy, zapada się. Powstałe wahania wody prowadzą do pojawienia się ogromnej liczby małych pęcherzyków powietrza w całej objętości wody: tak zwanego „białego klucza”.

Działa pęcherzyk powietrza o objętości na dnie naczynia siła podnoszenia:
Fpod \u003d Farchimede - Fgravity
Bańka jest dociskana do dna, ponieważ siły nacisku nie działają na dolną powierzchnię. Po podgrzaniu pęcherzyk rozszerza się z powodu uwolnienia do niego gazu i odrywa się od dna, gdy siła podnoszenia jest nieco większa niż siła nacisku. Wielkość bańki, która może oderwać się od dna, zależy od jej kształtu. Kształt pęcherzyków na dnie zależy od zwilżalności dna naczynia.
Niejednorodność zwilżania i zlewanie się pęcherzyków na dnie prowadziło do wzrostu ich wielkości. Na duże rozmiary Gdy za nią unosi się bańka, powstają puste przestrzenie, luki i wiry.
Kiedy bańka pęka, cała otaczająca ją ciecz wpada do środka i pojawia się fala pierścieniowa. Zamykając, wyrzuca słup wody.

Kiedy pękające bąbelki zapadają się w cieczy, rozchodzą się fale uderzeniowe o częstotliwościach ultradźwiękowych, którym towarzyszy słyszalny hałas. Do początkowe etapy wrzenie charakteryzuje się najgłośniejszymi i najwyższymi dźwiękami (na etapie „białego klawisza” czajnik „śpiewa”).
(źródło: virlib.eunnet.net)
WYKRES TEMPERATUR ZMIAN ZAGREGOWANYCH STANÓW WODY

ZOBACZ REGAŁ!
CIEKAWE
Dlaczego w pokrywce czajnika jest dziura?
Aby uwolnić parę. Bez dziury w pokrywce para może chlapać wodą na dziobek czajnika.
___
Czas gotowania ziemniaków od momentu ugotowania nie zależy od mocy grzałki. Czas trwania zależy od czasu przebywania produktu w temperaturze wrzenia.
Moc grzałki nie wpływa na temperaturę wrzenia, a jedynie na szybkość parowania wody.
Gotowanie może spowodować zamarznięcie wody. W tym celu konieczne jest wypompowanie powietrza i pary wodnej z naczynia, w którym znajduje się woda, tak aby woda cały czas wrzała.
"Garnki łatwo gotują się na krawędzi - na złą pogodę!"
Towarzyszący pogarszającej się pogodzie spadek ciśnienia atmosferycznego powoduje, że mleko szybciej „ucieka”.
___
Bardzo gorącą wrzącą wodę można uzyskać na dnie kopalń głębinowych, gdzie ciśnienie powietrza jest znacznie większe niż na powierzchni Ziemi. Tak więc na głębokości 300 m woda wrze w 101 ͦ C. Przy ciśnieniu powietrza 14 atmosfer woda wrze w 200 ͦ C.
Pod dzwonem pompy powietrza można dostać „wrzącą wodę” o temperaturze 20ͦC.
Na Marsie pilibyśmy „wrzącą wodę” o temperaturze 45 C.
Słona woda wrze powyżej 100 ͦ C. ___
W rejonach górskich na znacznych wysokościach, pod zmniejszonym ciśnieniem atmosferycznym, woda wrze w temperaturach niższych niż 100 ͦ Celsjusza.

Oczekiwanie na ugotowanie takiego posiłku trwa dłużej.
Wlej zimno ... i się zagotuje!
Normalnie woda wrze w 100 stopniach Celsjusza. Podgrzej wodę w kolbie na palniku do wrzenia. Wyłączmy palnik. Woda przestaje się gotować. Zamykamy kolbę korkiem i zaczynamy ostrożnie nalewać na korek zimną wodę. Co to jest? Woda znów się gotuje!
..............................pod odrzutowcem zimna woda w kolbie trochę wody, a wraz z nią para wodna zaczyna się ochładzać.
Zmniejsza się objętość pary i zmienia się ciśnienie nad powierzchnią wody...
Jak myślisz, w jakim kierunku?
... Temperatura wrzenia wody pod zmniejszonym ciśnieniem to mniej niż 100 stopni, a woda w kolbie znów się zagotuje!
____
Podczas gotowania ciśnienie wewnątrz garnka – „szybkowaru” – wynosi około 200 kPa, a zupa w takim garnku gotuje się znacznie szybciej.
Wodę można nabrać do strzykawki do około połowy, zamknąć ją tym samym korkiem i mocno pociągnąć za tłok. W wodzie pojawi się dużo bąbelków, co oznacza, że rozpoczął się proces gotowania wody (i to w temperaturze pokojowej!).
___
Gdy substancja przechodzi w stan gazowy, jej gęstość zmniejsza się około 1000 razy.
___
Pierwsze czajniki elektryczne miały pod spodem grzałki. Woda nie miała kontaktu z grzałką i gotowała się bardzo długo. W 1923 Arthur Large dokonał odkrycia: umieścił grzałkę w specjalnej miedzianej rurce i umieścił ją w czajniku. Woda szybko się zagotowała.
Puszki samoschładzające do napojów bezalkoholowych zostały opracowane w USA. W słoiku zamontowana jest komora z płynem niskowrzącym. Jeśli zmiażdżysz kapsułkę w upalny dzień, płyn zacznie gwałtownie wrzeć, odbierając ciepło zawartości słoika, a po 90 sekundach temperatura napoju spada o 20-25 stopni Celsjusza.
CZEMU?
Czy uważasz, że można ugotować jajko na twardo, jeśli woda wrze w temperaturze niższej niż 100 stopni Celsjusza?
____
Czy woda zagotuje się w garnku pływającym w innym garnku z wrzącą wodą?
Czemu? ___
Czy można zagotować wodę bez podgrzewania?

Wrzenie, jak widzieliśmy, jest również parowaniem, tylko towarzyszy mu szybkie tworzenie się i wzrost pęcherzyków pary. Oczywiste jest, że podczas gotowania konieczne jest doprowadzenie do cieczy pewnej ilości ciepła. Ta ilość ciepła trafia do tworzenia pary. Co więcej, różne ciecze o tej samej masie wymagają różnych ilości ciepła, aby zamienić je w parę w temperaturze wrzenia.
Eksperymenty wykazały, że odparowanie wody o wadze 1 kg w temperaturze 100°C wymaga 2,3 x 106 J energii. Do odparowania 1 kg eteru pobranego w temperaturze 35 °C potrzeba 0,4 10 6 J energii.
Dlatego, aby temperatura parującej cieczy nie uległa zmianie, do cieczy musi zostać doprowadzona pewna ilość ciepła.
Wielkość fizyczna pokazująca, ile ciepła jest potrzebne do przekształcenia cieczy o masie 1 kg w parę bez zmiany temperatury, nazywana jest ciepłem właściwym parowania.
Ciepło właściwe waporyzacji oznaczono literą L. Jego jednostką jest 1 J/kg.
Eksperymenty wykazały, że ciepło właściwe parowania wody w temperaturze 100°C wynosi 2,3 106 J/kg. Innymi słowy, do przekształcenia 1 kg wody w parę o temperaturze 100 °C potrzeba 2,3 x 106 J energii. Dlatego w temperaturze wrzenia energia wewnętrzna substancji w stanie pary jest większa niż energia wewnętrzna tej samej masy substancji w stanie ciekłym.
Tabela 6
Ciepło właściwe parowania niektórych substancji (w temperaturze wrzenia i przy normalnym ciśnieniu atmosferycznym)
W kontakcie z zimnym przedmiotem kondensuje para wodna (ryc. 25). W tym przypadku energia pochłonięta podczas tworzenia pary jest uwalniana. Dokładne eksperymenty pokazują, że po skondensowaniu para oddaje ilość energii, która została wykorzystana do jej powstania.

Ryż. 25. Kondensacja pary
W konsekwencji, gdy 1 kg pary wodnej zostanie przekształcony w temperaturze 100°C w wodę o tej samej temperaturze, uwalniane jest 2,3 x 106 J energii. Jak widać z porównania z innymi substancjami (tabela 6), energia ta jest dość wysoka.
Można wykorzystać energię uwolnioną podczas kondensacji pary. W dużych elektrowniach cieplnych para wykorzystywana w turbinach podgrzewa wodę.
Ogrzana w ten sposób woda wykorzystywana jest do ogrzewania budynków, łaźni, pralni oraz innych potrzeb domowych.
Aby obliczyć ilość ciepła Q potrzebnego do przekształcenia dowolnej masy cieczy pobranej w temperaturze wrzenia w parę, należy pomnożyć ciepło właściwe parowania L przez masę m:
Z tego wzoru można wywnioskować, że
m=Q/L, L=Q/m
Ilość ciepła uwalnianego przez parę o masie m, kondensującą w temperaturze wrzenia, określa się tym samym wzorem.
Przykład. Ile energii potrzeba, aby zamienić 2 kg wody o temperaturze 20°C w parę? Zapiszmy stan problemu i go rozwiążmy.

pytania
- Jaka jest energia dostarczana do cieczy podczas gotowania?
- Jakie jest ciepło właściwe waporyzacji?
- Jak można doświadczalnie wykazać, że energia jest uwalniana, gdy para się skrapla?
- Jaka jest energia uwalniana przez 1 kg pary wodnej podczas kondensacji?
- Gdzie w technologii wykorzystywana jest energia uwalniana podczas kondensacji pary wodnej?
Ćwiczenie 16
- Jak rozumieć, że ciepło właściwe parowania wody wynosi 2,3 10 6 J/kg?
- Jak rozumieć, że ciepło właściwe kondensacji amoniaku wynosi 1,4·106 J/kg?
- Która z substancji wymienionych w tabeli 6, po przekształceniu ze stanu ciekłego w parę, ma większy wzrost energii wewnętrznej? Uzasadnij odpowiedź.
- Ile energii potrzeba, aby zamienić 150 g wody w parę o temperaturze 100°C?
- Ile energii trzeba zużyć, aby woda o masie 5 kg pobrana w temperaturze 0°C zagotowała się i odparowała?
- Jaką ilość energii uwolni woda o masie 2 kg po schłodzeniu ze 100 do 0 °C? Jaka ilość energii zostanie uwolniona, jeśli zamiast wody weźmiemy taką samą ilość pary o temperaturze 100°C?
Ćwiczenie
- Zgodnie z tabelą 6 określ, która z substancji po przekształceniu ze stanu ciekłego w parę, energia wewnętrzna wzrasta silniej. Uzasadnij odpowiedź.
- Przygotuj raport na jeden z tematów (opcjonalnie).
- Jak powstaje rosa, mróz, deszcz i śnieg.
- Obieg wody w przyrodzie.
- Odlewanie metali.
